Antwoord vraag 1: C
Toelichting
Capnocytophaga canimorsus is een gramnegatieve staaf die behoort tot de commensale flora van de orofarynx van onder andere honden en katten. De bacterie kan bij mensen levensbedreigende infecties veroorzaken met een fulminant beloop, meestal in de vorm van sepsis, maar ook als meningitis, endocarditis en soms als endoftalmitis. Risicofactoren voor infectie zijn asplenie, alcoholmisbruik, een recente hondenbeet of nauw contact met honden en/of katten. C. canimorsus vereist voor optimale groei een anaeroob of micro-aerofiel milieu. Voor de groei is een verlengde incubatietijd nodig. De kolonies groeien veelal pas na 4 tot 14 dagen en ogen op bloed- en chocolade-agar als kleine geel/oranje waterige kolonies. De bacterie groeit slecht op Mac Conkey agar.1
De meest recent gepubliceerde studie naar het vóórkomen van C. canimorsus in Nederland laat in totaal 32 patiënten zien in de periode 2003-2005, wat resulteert in een jaarlijkse incidentie van 0,63 per miljoen. In 30 gevallen werd de diagnose gesteld via een positieve kweek (bij 29 patiënten uit bloed, één zowel uit bloed als liquor en één van een conjunctivale kweek).2
Een studie van een referentielaboratorium uit Californië rapporteerde 56 C. canimorsus-isolaten in de periode van 1972 tot 2004. De confirmaties zijn uitgevoerd via een combinatie van conventionele en moleculaire technieken, waaronder biochemische testen, vetzuuranalyse en 16S rRNA gen sequencing. In 51 gevallen werd de bacterie geïsoleerd uit bloed, in vier gevallen uit liquor en in één geval uit de keel. 13 procent van de ingestuurde isolaten werd aanvankelijk verkeerd geïdentificeerd, het meest waarschijnlijk door de beperkte diagnostische mogelijkheden van destijds. In totaal werden zes patiënten in eerste instantie opgenomen met het beeld van een cellulitis. In alle gevallen werd de bacterie gekweekt uit bloed, maar niet uit de wonden.3 Ook in een studie van het Centre for Disease Control uit 1989 waren van de 150 opgestuurde stammen er slechts drie (twee procent) afkomstig uit wonden, terwijl 88 procent afkomstig was uit bloedkweken.4 Daarnaast is gezien de trage groei de wondkweek niet de snelste methode om de verdenking te ondersteunen.3
Daarmee zijn er nog drie antwoordopties over: 16s PCR op volbloed, een bloedkweek of een direct preparaat van volbloed. De studie uit Californië gebruikte zowel bloedkweken als een 16s PCR techniek op bloed uit een bloedkweekflesje om de diagnose te stellen, waarmee optie A en B dus mogelijk zijn. Verschillende case reports laten zien dat het mogelijk is om C. canimorsus te vinden in directe preparaten van volbloed.5-7 Een preparaat op volbloed toont dunne gramnegatieve staven met spitse uiteinden. De bacterie vertoont een karakteristieke motiliteit, wat als ‘gliding motility’ wordt beschreven.
Zowel een 16s PCR, een bloedkweek als een direct preparaat van volbloed kan dus de verdenking op een C. canimorsus-infectie ondersteunen dan wel bevestigen. Helaas is er weinig literatuur over de sensitiviteit van deze methoden. Van deze opties is optie C, een direct preparaat op volbloed, de snelste optie en daarmee het juiste antwoord op de vraag.
Antwoord vraag 2: A
Toelichting
Volgens de WIP-richtlijn 'Indicaties voor isolatie' is er geen isolatie geïndiceerd voor een patiënt met tularemie.8
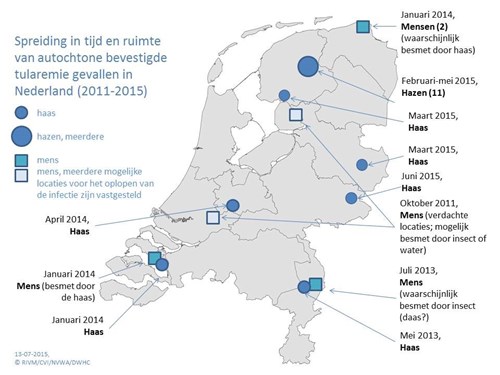
Tularemie is een zoönose die wordt veroorzaakt door de bacterie Francisella tularensis, een pleiomorfe gramnegatieve coccobacil.9 F. tularensis komt met name voor op het noordelijk halfrond en bestaat uit verschillende subspecies, waarbij de meeste humane infecties worden veroorzaakt door de subspecies tularensis (vooral Noord-Amerika) en holarctica (vooral Europa).10 F. tularensis subsp. tularensis is pathogener dan F. tularensis subsp. Holarctica.9,10 In Nederland komen infecties sporadisch voor, waarbij 21 humane gevallen gemeld zijn sinds 2011 (figuur 1).11,12 F. tularensis is een van de meest virulente bacteriën, waarbij de infectieuze dosis 10-50 bacteriën betreft, en wordt dan ook gezien als mogelijk bioterroristisch wapen.9,10,13
In de literatuur zijn verschillende besmettingswegen beschreven:9,10
- Contact met geïnfecteerde dieren(vlees), met name hazen, konijnen en knaagdieren (woelmuizen)
- Beten/steken van insecten (dazen, teken en muggen)
- Via het milieu (bijvoorbeeld besmet drinkwater)
- Inhalatie van aerosolen (bijvoorbeeld bij hooi- en maaiwerkzaamheden)
- Er is zeer sporadisch besmetting van mens op mens beschreven.
In de meeste gevallen verloopt de besmetting door contact met geïnfecteerde dieren. Om deze reden staat het ziektebeeld ook wel bekend als ‘Rabbit fever´. Afhankelijk van de manier en dosis van infectie, immuunstatus van de patiënt en subspecies, kunnen zeven ziektebeelden onderscheiden worden (ulceroglandulair, glandulair, oculoglandulair, orofaryngeaal, intestinaal, tyfoïdaal en pulmonaal).9,10 De ulceroglandulaire vorm komt het meeste voor en wordt gekenmerkt door een ulcererende papel in combinatie met regionale lymfadenopathie.
F. tularensis kan gekweekt worden uit verschillende klinische monsters (bloed, pus, respiratoir materiaal, weefsel).10 Het is een obligaat aerobe, langzaamgroeiende bacterie, die het beste groeit op cysteïne-bevattende agars, meestal beter groeit op chocolade- dan bloedagar, en niet op MacConkey agar.9,13 F. tularensis subsp. tularensis is een BSL-3 micro-organisme vanwege mogelijk gebruik voor bioterrorisme, maar F. tularensis subsp. holarctica kan onder BSL-2 condities verwerkt worden.10 Er zijn casus beschreven waarbij F. tularensis door laboratoriummedewerkers werd opgelopen door manipulatie van een kweek waarbij aerosolen ontstonden.14 Determinatie is mogelijk via MALDI-TOF (indien de MALDI-TOF-database F. tularensis-spectra bevat, en zelfs dan kan determinatie moeilijk zijn)15 of PCR. Serologie is bruikbaar vanaf 10 tot 20 dagen na infectie, waarbij hoge titers tot jaren na infectie kunnen persisteren.9
Tot dusverre is er sporadisch casuïstiek beschreven van mens-op-menstransmissie van F. tularensis. De eerste mogelijke casus stamt uit 1924 waarbij een moeder tularemie opliep nadat ze in haar duim prikte toen ze een tularemie-ulcus bij haar zoon probeerde te manipuleren met een naald.16 Een tweede casus vermeldt overdracht van F. tularensis tijdens een autopsie van een patiënt die overleed aan tularemie.17 Recent is overdracht van F. tularensis beschreven ten gevolge van orgaantransplantatie.18 In alle gevallen betreft het overdracht via direct bloedcontact. Omdat er geen verspreiding van mens op mens via aerosolen, druppels of direct contact is beschreven, is er geen indicatie voor isolatie van een opgenomen patiënt in het ziekenhuis. Wel is tularemie een meldingsplichtige ziekte groep C, waarbij de GGD een vragenlijst zal afnemen om de besmettingsbron te achterhalen, zodat er gekeken kan worden voor wie of voor welke risicogroepen aanvullend preventieve maatregelen nodig zijn.9