Samenvatting
De medische mycologie is een dynamisch veld met vele ontwikkelingen. De taxonomie van schimmels ondergaat een revolutie door de toepassing van moleculaire methoden. Taxonomische revisies leiden tot meer diversiteit, zoals bijvoorbeeld bij Aspergillus fumigatus, terwijl bij andere soorten weinig diversiteit wordt gevonden zoals bij Rhizopus-species. Revisie van het genus Cryptococcus heeft ertoe geleid dat het aantal soorten sterk is gereduceerd naar zeven soorten die humaan pathogeen zijn. Met behulp van Malditof en moleculaire technieken kunnen cryptokokken van elkaar worden onderscheiden. Moleculaire technieken dragen ook bij tot een beter inzicht in de verwekkers van Madura-voet, een ziekte die verantwoordelijk is voor een significante ziektelast in (sub)tropische regionen. Voor de behandeling wordt vooruitgang geboekt met het uitproberen van bestaande en nieuwe middelen. Candida auris is een recent ontdekte, fluconazol-resistente gist die invasieve infecties kan veroorzaken. De gist is geassocieerd met uitbraken, reden waarom stringente hygiënemaatregelen noodzakelijk zijn. Resistentie speelt ook een steeds grotere rol bij A. fumigatus-infecties, en de SWAB heeft recent de richtlijn aangepast en vastgelegd dat combinatietherapie een grote rol speelt bij de primaire behandeling van invasieve aspergillose. In juli 2018 wordt het mondiale ISHAM-congres gehouden in Amsterdam, waar bovenstaande en vele andere schimmelproblemen zullen worden besproken.
Summary
Medical mycology is a dynamic field with many new developments. The use of molecular techniques has revolutionized the taxonomy, sometimes showing higher diversity than expected, for instance in Aspergillus fumigatus, and sometimes lower diversity like in Rhizopus species. Revision of the taxonomy of Cryptococcus has resulted in an important reduction of the number of species, to seven that are involved in human disease. Malditof and molecular methods enable reliable differentiation of the various species. Molecular methods also contribute to a better understanding of Madura-foot, a condition that causes significant morbidity in (sub)tropical regions. Drug discovery programs have been developed aimed at evaluating existing and new antifungal compounds in order to improve treatment. Candida auris is a recently described, fluconazole-resistant yeast that may cause invasive candidiasis. The yeast is associated with outbreaks and therefore stringent hygiene measures are warranted when identified. Resistance also plays an increasing role in infections caused by A. fumigatus, and the Dutch guideline was recently revised now recommending combination therapy as primary treatment option in patients with invasive aspergillosis. In July 2018 the global ISHAM conference will be held in Amsterdam where abovementioned and many other fungal disease issues will be discussed.
Inleiding
Er zijn in Nederland verschillende instellingen en onderzoeksgroepen die zich richten op schimmels en schimmelinfecties.
De medische mycologie is een dynamisch veld met vele ontwikkelingen zowel in Nederland als wereldwijd, met aspergillose en gistinfecties als belangrijkste probleemgebieden; de laatste tijd zien we ook veel infecties door Fusarium- species en door Mucorales. Mondiaal gezien zijn vooral cryptokokkose, chromoblastomycose, sporotrichose, systemische fungi en madura-voet actueel.
Schimmelinfecties worden al bestudeerd sinds 1840, en op dit moment zijn ongeveer 625 soorten bekend.1 Dat lijkt veel, maar het is slechts een fractie van het aantal bestaande schimmels, dat op enkele miljoenen wordt geschat. Pathogene en opportunistische schimmels moeten heel bijzondere eigenschappen hebben, want het veroorzaken van een infectie, zelfs bij een ernstig zieke patiënt, is helemaal niet zo makkelijk.
Taxonomie
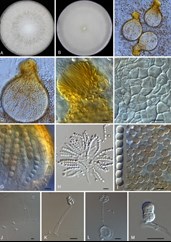
De taxonomie van schimmels ondergaat momenteel een revolutie door de toepassing van moleculaire methoden, die de morfologie, die 150 jaar lang zo betrouwbaar leek, in rap tempo aan het vervangen zijn. Schimmels die er hetzelfde uitzien kunnen tot heel andere soorten behoren, en microscopisch compleet verschillende structuren kunnen vormen zijn van eenzelfde soort. We moeten met de taxonomie van medische schimmels grotendeels opnieuw beginnen. Een probleem daarbij is de inherente instabiliteit van de methodiek. Indelingen zijn nu een reflectie van moleculaire stambomen, dus afstanden van species ten opzichte van elkaar. Conclusies kunnen dus verschillen al naar gelang de soorten die worden vergeleken. Ook kennen we de richting van de stamboom niet, we weten bijna nooit welke soorten we als primitief moeten beschouwen en welke als hoger geëvolueerd. Dit leidt ertoe dat haast elk taxonomisch artikel naamsveranderingen voorstelt: sommige soorten zijn het laatste decennium vijfmaal van naam veranderd en het einde is nog niet in zicht. Een voorbeeld van onverwachte fylogenetische verbanden vinden we in Fusarium, waar een deel van de soorten nauw verwant blijkt te zijn met de fraaie ascomyceten in Neocosmospora (zie figuur 1). Of we een overbekende soort als Fusarium solani voortaan Neocosmospora solani moeten noemen is een punt van discussie.
Moleculaire methoden zijn spectaculair nauwkeuriger dan morfologie. Overbekende soorten als A. fumigatus bleken meerdere soorten te omvatten. A. lentulus werd vroeger doorgaans behandeld als een gedegenereerde A. fumigatus, maar onderscheid tussen soorten is van praktisch belang vanwege verschillen in thermotolerantie en antifungale gevoeligheid. Een eeuw lang werd gedacht dat sporotrichose werd veroorzaakt door één enkele soort, Sporothrix schenckii, maar deze blijkt uit vier nauw verwante maar duidelijk verschillende soorten te bestaan, die verschillen in virulentie en resistentie voor antimycotica. Heel bijzonder is dat ze ook verschillen in hun transmissieroutes: Sporothrix globosa komt voor op rottend plantenmateriaal, maar S. brasiliensis wordt verspreid via de nagels van straatkatten.
Het komt ook voor dat de diversiteit juist kleiner is dan gedacht. Er blijken maar een paar Rhizopus-species te bestaan; veel vroegere namen, vaak van soorten die worden gebruikt voor de bereiding van voedingsmiddelen, zijn nu synoniemen van algemeen voorkomende soorten als Rhizopus microsporus en R. arrhizus – waarmee klinische en voedselgerelateerde stammen tot dezelfde soort behoren. Een apart geval is Fusarium, die we steeds vaker tegenkomen in de kliniek, zowel in oppervlakkige als in systemische infecties.2 De moleculaire diversiteit van deze groep is enorm en er wordt nog gediscussieerd of het zinvol is elke moleculaire variant als een aparte soort te beschrijven.
Cryptokokkose
Cryptokokkose is de verzamelnaam voor infecties die worden veroorzaakt door basidiomycete gisten die tot de Cryptococcus neoformans/Cryptococcus gattii-soortscomplexen behoren. Begin tachtiger jaren steeg wereldwijd het aantal Cryptococcus-infecties sterk door de hiv-pandemie, maar de introductie in 1995 van de highly active anti-retroviral therapy zorgde voor een afname van cryptokokkenmeningitis.3,4 Een recente studie becijferde dat er wereldwijd jaarlijks circa 220.000 nieuwe gevallen van hiv-geassocieerde cryptokokkenmeningitis worden gediagnosticeerd, circa driekwart van deze patiënten leeft in zuidelijk Afrika.3 Dezelfde studie berekende dat jaarlijks ongeveer 181.000 individuen overlijden aan een cryptokokkenmeningitis, wereldwijd is cryptokokkose daarmee verantwoordelijk voor 15 procent van de aidsgerelateerde doodsoorzaken.3 Hoewel cryptokokken veelal worden gezien als opportunistische ziekteverwekkers blijkt dat er in toenemende mate infecties worden vastgesteld bij ogenschijnlijk immuuncompetente individuen, dit kwam ook naar voren bij een retrospectieve Nederlandse epidemiologische studie uitgevoerd over de periode 1977 tot 2007.4 C. gattii sensu lato wordt veelal gerelateerd aan tropische en subtropische klimaatzones, maar naast diverse reisgerelateerde infecties zijn er ook enkele Nederlandse autochtone casussen bekend.4
Voor de diagnostiek van cryptokokkeninfecties zijn naast de conventionele methoden van kweek, serologie en Indische inktpreparaat ook nieuwere methoden beschikbaar, zoals de laterale flow assay en Malditof. Daarnaast zijn er (commerciële) moleculair diagnostische tests beschikbaar, veelal aangeboden in een ‘syndrome panel’ voor het detecteren van meningitis-veroorzakende ziekteverwekkers. Met behulp van Malditof en moleculaire technieken kunnen de verschillende soorten cryptokokken van elkaar worden onderscheiden, hoewel hiervoor bij gebruik van de Malditof er een geactualiseerde versie van de identificatieprogrammatuur nodig is om tot een betrouwbare uitslag te komen voor met name de soorten in het C. gattii-soortencomplex.5,6
De opkomst van moleculaire typeringstechnieken heeft bijgedragen aan verfijning van de taxonomie van het genus Cryptococcus, een recente taxonomische revisie heeft ertoe geleid dat het aantal soorten sterk is gereduceerd van ruim honderd naar slechts tien soorten waarvan er zeven humaan pathogeen zijn.6 De afgelopen decennia zijn gegevens verzameld om een taxonomische revisie van de C. neoformans/C. gattii-soortscomplexen te ondersteunen, met name vanuit een klinisch oogpunt. Gecombineerd met fenotypische, ecologische, geografische en epidemiologische karakteristieken zijn de C. neoformans variëteiten grubii en neoformans verheven tot de soorten C. neoformans (serotype A) en C. deneoformans (serotype D), terwijl C. gattii is opgesplitst in vijf soorten op basis van de bekende genotypen: C. gattii sensu stricto (serotype B; wereldwijd), C. bacillisporus (serotype B/C; hiv-geassocieerd; met name Noord- en Zuid-Amerika), C. deuterogattii (serotype B; wereldwijd voorkomen, diverse uitbraken), C. tetragattii (serotype C; hiv-geassocieerd; Afrika en India) en C. decagattii (serotype B; hiv-geassocieerd; Centraal-Amerika).6
Hoewel er voor de kliniek potentieel relevante verschillen waarneembaar zijn tussen de verschillende soorten, zoals in vitro-antifungale gevoeligheid en gastheereigenschappen, vinden sommige clinici en onderzoekers dat deze herziene naamgeving te vroeg is uitgevoerd en zij houden daarom vast aan de term soortscomplexen.7 Maar juist het gebruik van de herziene naamgeving zal voortschrijdend inzicht verschaffen in de voor de patiënt relevante eigenschappen van deze soorten.8
Mycetoominfecties
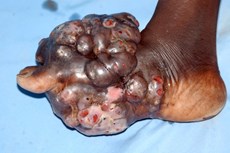
Mycetoom is een subcutane infectieziekte, die gekenmerkt wordt door grote tumorachtige gezwellen met name op de voet (zie figuur 2). Deze infectieziekte kan worden veroorzaakt door verschillende micro-organismen, zowel door bacteriën (actinomycetoma) als door schimmels (eumycetoma). Deze infectieziekte komt met name voor in tropische en subtropische regionen en werd pas in 2016 als zogenaamde neglected tropical disease (NTD) erkend door de Wereldgezondheidsorganisatie. Hoewel mycetoom dus met name in de tropen voorkomt, zijn er ook mycetoompatiënten in Frankrijk, Engeland en zelfs Nederland beschreven, met name bij immigranten.9
Omdat mycetoom eerder niet als NTD was erkend, is er een gebrek aan goede diagnostische testen en behandeling. Mycetoom kan worden veroorzaakt door 70 verschillende micro-organismen en de identificatie is gebaseerd op kweek. De meeste fungale veroorzakers laten echter geen enkele vorm van sporulatie zien waardoor misidentificaties vaak voorkomen, niet alleen in de endemische gebieden. Recentelijk bleek na moleculaire identificatie dat 78 procent van de isolaten afkomstig van Britse en Franse referentiecollecties fout waren geïdentificeerd.10 Tevens bleek dat de taxonomie van de veroorzakers van mycetoom niet juist was, hetgeen recentelijk door het Westerdijkinstuut is gecorrigeerd.11,12 Ook in de endemische gebieden zelf blijken misidentificaties veel voor te komen. Daarom wordt op dit moment in een klinische studie in Soedan vastgesteld of species-specifieke PCR’s een betere en snellere diagnostiek opleveren bij mycetoma.13
Correcte identificatie van het veroorzakende micro-organisme is van belang voor de behandeling van mycetoma. Actinomycetoma wordt behandeld met antibiotica, meestal een combinatie van trimethoprim-sulfamethoxazole en amikacinesulfaat toegediend in cycli van vijf weken. Deze therapie leidt bij 90 procent van de patiënten tot genezing. Eumycetoom wordt behandeld gedurende zes maanden met itraconazol, gevolgd door het chirurgisch weghalen van de laesie en een additionele therapie van zes maanden itraconazol. Helaas leidt dit bij 25 tot 50 procent van de gevallen tot het terugkomen van de infectie en bij 2,8 tot 25 procent van de patiënten uiteindelijk tot amputatie van het aangedane ledemaat. Daarom is het Erasmus MC sinds 1999 bezig om betere geneesmiddelen voor mycetoom te vinden. Dit begon met het ontwikkelen van een in vitro-gevoeligheidstest waarbij hyfen als startpunt worden gebruikt. De azolen leken de beste in vitro-activiteit te hebben voor de meeste veroorzakers, alleen Madurella fahalli en Medicopsis romeroi bleken niet gevoelig te zijn voor itraconazol.12,14 Met behulp van deze test hebben we ook aangetoond dat het azool ravuconazole de beste in vitro-activiteit had tegen Madurella mycetomatis, de meest voorkomende verwekker. Deze bevinding heeft geleid tot de eerste klinische studie naar de behandeling van mycetoom waarbij de effectiviteit van fosravuconazol (een prodrug van ravuconazol) wordt vergeleken met itraconazol. Daarnaast hebben we een Mycetoma Open Source (MycetOS) drugdiscoveryprogramma opgezet, met als doel het identificeren van nieuwe klassen mycetomaremmers. In dit licht zijn 800 middelen in vitro gescreend en werden 215 potentiële nieuwe middelen ontdekt. In vivo is verder gekeken of deze middelen ook enige activiteit vertoonden in een invertebraat mycetoommodel. In dit model worden larven van de wasmot Galleria mellonella geïnfecteerd en vormen zich binnen vier uur al korrels.15 Eerst zijn de gebruikelijke antifungale middelen getest en het bleek dat in tegenstelling tot de in vitro-gevoeligheden juist amfotericine B en terbinafine een betere overleving gaven dan de azolen. Dit werd naderhand bevestigd in een muismodel. Ook werden uit de nieuw geïdentificeerde moleculen nieuwe stoffen geïdentificeerd, die op dit moment verder worden onderzocht.
Candida auris
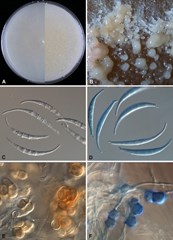
Candida auris is een pas minder dan 10 jaar geleden beschreven gist die is geassocieerd met invasieve infecties in ziekenhuizen en verpleeghuizen. Deze fluconazol-resistente gist werd het eerst gesignaleerd in Azië, Zuid-Afrika en Latijns-Amerika maar recent zijn er ook ziekenhuisuitbraken gerapporteerd in Europa en de VS.16 Deze uitbraken bleken heel moeilijk onder controle te krijgen ondanks implementatie van zeer strikte infectiepreventie. In tegenstelling tot andere Candida-soorten lijkt C. auris bijzonder gemakkelijk van patiënt op patiënt overdraagbaar te zijn, waarschijnlijk door omgevingscontaminatie en kolonisatie van patiënten en ziekenhuispersoneel.17 Veel fenotypische commerciële identificatiemethoden die in microbiologische laboratoria worden gehanteerd, zijn ongeschikt om C. auris correct te identificeren.
Het is een goed gebruik om Candida-soorten, geïsoleerd bij invasieve infecties, tot op speciesniveau te identificeren. C. auris is kiembuisnegatief, net zoals de meeste non-albicanssoorten, de koloniekleur is bleek-paars tot roze op CHROMagar Candida medium en de gisten kunnen beter bij hogere temperaturen groeien dan de meeste Candida-soorten. C. auris wordt meestal goed geïdentificeerd met Malditof, mits de databank actueel is. DNA-sequentiëring van D1/D2 is ook een goede methode. Identificatie van C. auris met vier biochemische testen liet zien dat alle C. auris-isolaten fout werden geïdentificeerd; namelijk als Rhodotorula glutinis of C. haemulonii met API-20C AUX, als C. haemulonii met Phoenix en met Vitek-2, en als C. famata, C. lusitaniae, C. guilliermondii, of C. parapsilosis door MicroScan (Beckman-Coulter). Het is dan zaak om Malditof of DNA-sequentiëring toe te passen. Als Candida-isolaten ook worden getest voor in vitro-gevoeligheid dan is fluconazol-resistentie een karakteristiek kenmerk dat een aanleiding moet zijn om een correcte identificatie uit te voeren.18
Samenvattend, er moet aan C. auris worden gedacht bij de volgende bevindingen:
- moeilijk te behandelen infectie zonder reactie op fluconazol;
- meerdere gevallen van gistinfectie op een afdeling of unit;
- fluconazol-resistente non-albicansisolaten bij urine- en bloedkweken.
Goede standaardhygiëne en infectiepreventie, voldoende isolatiekamers en goede terminale desinfectie van kamers zijn noodzakelijk om uitbraken met C. auris in ziekenhuizen en verpleeghuizen te voorkomen. Toename van invasieve infecties door non-albicanssoorten die fluconazol-resistent zijn en patiënten overgeplaatst uit ziekenhuizen (vooral Azië en Midden-Oosten) met C. auris-uitbraken zijn verdacht. C. auris gedraagt zich als BRMO’s (denk aan VRE) en C. auris-patiënten moeten worden geïsoleerd voor de gehele duur van de opname, zeker ook omdat effectieve dekolonisatie met bijvoorbeeld chloorhexidine twijfelachtig effect heeft.
Het aantonen van slechts een enkele casus is aanleiding voor een ringonderzoek (medepatiënten inclusief mogelijk omgevingskweken). Bij twee of meer patiënten dient het onderzoek te worden uitgebreid over de hele afdeling (denk mogelijk ook aan afdelingen waar veel patiënten mee worden gedeeld). Omdat het niet mogelijk is om medewerkers te dekoloniseren is het niet zinvol hen te onderzoeken op dragerschap, tenzij ze huid- of nagelinfecties hebben die kunnen passen bij Candida-infecties.
Ofschoon de meest adequate kweekplaatsen niet bekend zijn lijkt het erop dat surveillancekweken het beste worden afgenomen van plaatsen waar andere BRMO ook worden gezocht: neus/keel, lies, oksel, rectum/perianaal, insteekopeningen van intravasculaire lijnen en klinisch materiaal zoals urine, feces, luchtwegmateriaal en wondkweken.
Het is belangrijk om alle artsen-microbioloog en internisten-infectioloog ervan te doordringen dat C. auris ook, op korte of lange termijn, in Nederland zal opduiken. De vraag is of alle microbiologische laboratoria betrouwbaar C. auris kunnen identificeren. Het is dus zaak om goed voorbereid te zijn en bedacht te zijn op epidemische verspreiding in ziekenhuizen. Het Expertisecentrum Schimmelinfecties Radboudumc/CWZ heeft in overleg met het CiB/RIVM recent referentiematerialen naar Nederlandse laboratoria gestuurd om te waarborgen dat ze C. auris kunnen herkennen. Dit kan ertoe leiden dat er stammen worden aangetroffen in opgeslagen collecties in Nederlandse laboratoria. In zowel Nijmegen (Radboudumc/CWZ) als Groningen zijn geen C. auris-isolaten gevonden in Candida-collecties tot 2000. Een enkele isolatie van C. auris uit klinisch materiaal zal een aanleiding moeten zijn tot isolatie van de betrokken patiënt en het verrichten van ringonderzoek op de afdeling. Het Expertise Centrum Schimmelinfecties Radboudumc/CWZ kan assisteren bij identificatie, gevoeligheidsbepaling en zal desgevraagd adviseren bij brononderzoek. Tot slot verdient het aanbeveling om bewezen C. auris-infecties/kolonisaties voorlopig centraal, bij voorkeur CiB/RIVM, te melden.
Invasieve aspergillose en resistentie
Aspergillose is een verzameling van ziekten veroorzaakt door Aspergillus-species. In Nederland worden de meeste infecties veroorzaakt door A. fumigatus, maar andere species worden soms gekweekt bij specifieke patiëntengroepen of uit bepaalde materialen. Zo wordt A. nidulans vaak gevonden bij invasieve infecties bij patiënten met chronisch granulomateuze ziekte (CGD) en A. niger bij patiënten met chronische otitis of een radicaalholte. Invasieve aspergillose (IA) en chronische pulmonale aspergillose (CPA) worden vaak veroorzaakt door A. fumigatus, een saprofytaire schimmel die graag groeit op dood plantaardig materiaal (compost). De schimmel is thermotolerant en kan temperaturen tot 50° C weerstaan. Hoewel IA voorkomt bij klassieke risicopatiënten zoals patiënten met hematologische maligniteiten (acute myeloïde leukemie, acute lymfoblastische leukemie, allogene stamceltransplantatie) en orgaantransplantatie, worden in toenemende mate invasieve infecties gezien bij patiënten opgenomen op de intensive care (IC). Recent onderzoek toont aan niet alleen patiënten met COPD en andere chronische longziekten maar ook patiënten met ernstige influenza een hoog risico hebben op IA. Een onderzoek bij IC-patiënten in de acht Nederlandse universitaire medische centra (umc’s) in het griepseizoen 2015/2016 toonde een prevalentie van 16 procent,19 terwijl een tweede onderzoek over meerdere griepseizoenen in zeven Nederlandse en Belgische ziekenhuizen een prevalentie van 19 procent liet zien.20 Opvallend hierbij is dat ook patiënten die voorheen gezond waren, dus zonder bekende risicofactoren, IA ontwikkelden.19,20 Ook werd vaak een aspergillus-tracheobronchitis gevonden, die een andere klinische en radiologische presentatie heeft dan de infectie van het longparenchym.19
Naast nieuwe patiëntengroepen speelt azoolresistentie een steeds grotere rol bij infecties door A. fumigatus. Surveillanceonderzoek in vijf umc’s toont een resistentiefrequentie van 12,9 procent bij ongeselecteerde klinische A. fumigatus-isolaten.21 Hogere resistentiefrequenties werden gevonden bij specifieke patiëntengroepen zoals IC-patiënten met IA.22 Antimicrobiële resistentie, tot recent vooral gelijkgesteld aan antibacteriële resistentie, omvat ook antifungale resistentie. Een 'one healt'-oplossing voor Aspergillus- resistentie moet vooral ook gezocht worden in het milieu.23 Azoolresistentie wordt gedomineerd door mutaties die zich ontwikkelen door blootstelling aan azoolfungiciden die worden gebruikt in het milieu. A. fumigatus is daarbij niet het doelorganisme maar sommige fungiciden hebben anti-aspergillusactiviteit waaraan de schimmel wordt blootgesteld wanneer zich residuen bevinden in organisch afval, zogenaamde ‘hotspots’. Deze hotspots zijn mogelijk een bron voor resistente infectie bij de mens, maar nader onderzoek is nodig om deze relatie te bevestigen en de effectiviteit van maatregelen te onderzoeken.24
Klinische consequenties van azoolresistentie is dat elke patiënt die wordt verdacht van IA een resistente infectie kan hebben. Recent onderzoek toonde een absolute letaliteittoename door azoolresistentie van 31 procent bij hematologische patiënten en van 20 procent bij een ziekenhuisbrede patiëntenpopulatie.25 Ook werd duidelijk dat patiënten met een voriconazol-resistente IA die initiële behandeling ontvingen met voriconazol en vervolgens werden behandeld met een effectief middel, toch een hogere sterfte hadden dan patiënten die meteen adequate behandeling ontvingen. Deze inzichten hebben ertoe geleid dat de SWAB-richtlijn voor IA is aangepast, waarbij resistentie wordt meebehandeld bij patiënten verdacht voor IA.26 Dit betekent combinatietherapie van voriconazol of isavuconazol met een echinocandine of liposomaal amfotericine B. Alleen bij weinig ernstige infecties waarbij resultaten van resistentieonderzoek snel bekend zijn, kan met voriconazol- or isavuconazol-monotherapie worden begonnen. De detectie van resistentie is moeilijk vanwege de lage opbrengst van de kweek. Resistentie-PCR in BAL is mogelijk, waarbij de aanwezigheid van twee resistentiemutaties direct kan worden aangetoond, maar de gevoeligheid van deze test is ook beperkt.27
Congres van de ISHAM
In Nederland is de medische mycologie georganiseerd in een vereniging, de Vereniging voor Medische Mycologie (NvMy). De vereniging verwelkomt leden die interesse hebben in de medische mycologie zoals medisch specialisten, onderzoekers en analisten. Ze organiseert bijeenkomsten en cursussen op het gebied van de medische mycologie en is vertegenwoordigd in verschillende internationale mycologieverenigingen, zoals de European Confederation for Medical Mycology (ECMM) en de International Society for Human and Animal Mycology (ISHAM).
 |
In 2018 mag de NvMy als gastheer optreden voor het congres van de ISHAM dat plaatsvindt in Amsterdam van 30 juni tot en met 4 juli. Er worden meer dan 1000 deelnemers verwacht vanuit alle windstreken. Het congres zal ruimte bieden aan de humane en veterinaire mycologie in de volle breedte, van fundamenteel tot translationeel en klinisch. Een mooie gelegenheid om de mycologie in Nederland te etaleren, maar ook interessant voor degenen die zich niet dagelijks bezighouden met schimmelproblematiek.