Samenvatting
In het laatste decennium wordt steeds duidelijker dat pathogene micro-organismen zich niet houden aan gastheerspeciesbarrières, met zoönotische uitbraken die jaar na jaar plaatsvinden. Het hepatitis E-virus (HEV) was lang bekend als oorzaak van non-A-, non-B-hepatitis in ontwikkelingslanden, maar is pas de laatste jaren bekend als zoönose. Een zoönose, die in geïndustrialiseerde landen endemisch is en wordt geassocieerd met een chronisch ziektebeeld bij immuungecompromitteerde patiënten en met extrahepatische symptomen met ernstige gevolgen. Het virus vormt een gezondheidsrisico en zou daarom bestreden moeten worden. Doordat HEV verschillende transmissieroutes heeft, is een multidisciplinaire aanpak met een ‘one health’-gedachte nodig.
Summary
In the last decade it is becoming more clear that pathogenic micro-organisms do not adhere to host-species boundaries, resulting in the increasing occurrence of zoonotic epidemics. Hepatitis E virus was long known as the agent causing non-A, non-B hepatitis in developing countries, but only recently as a zoonotic pathogen. This zoonosis is endemic in industrialised countries and associated with chronic hepatitis in immune compromised patients and extra-hepatic symptoms with major clinical impact. This virus poses a health risk and should therefore be battled. However, due to the many transmission routes, this can only be achieved by a one-health approach.
Inleiding
In het afgelopen decennium zijn we in toenemende mate geconfronteerd met virussen die vanuit het dierenrijk de sprong naar de humane gastheer hebben gemaakt en daarmee (grote) uitbraken veroorzaakten. De meest bekende voorbeelden, naast het al bekende influenzavirus, zijn SARS (2003) en MERS (2012)-coronavirussen, ebolavirus (2014/2015) en afgelopen jaar, zikavirus. Een voorbeeld van een meer verraderlijke zoönose is het hepatitis E-virus (HEV), dat in toenemende mate erkend is als veroorzaker van infecties van zoönotische aard. Het is endemisch bij varkens en in wildedierenreservoirs over de hele wereld. Met recht een virus dat alleen door een ‘one health’-benadering bestreden zou kunnen worden.
Hepatitis E-virus
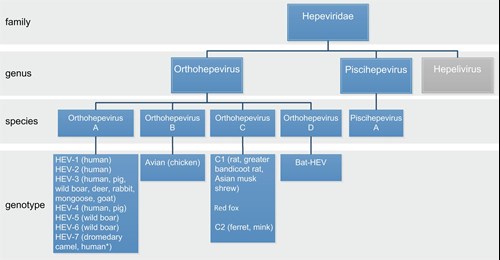
Hepatitis E is al lang bekend als oorzaak van hepatitis bij de mens. In de 18e eeuw zijn grote epidemieën beschreven met geelzucht, die opvielen door extreem hoge mortaliteit bij zwangere vrouwen. In 1983 is de virale verwekker ontdekt.1 HEV behoort tot de familie Hepeviridae, met de drie genera Orthohepevirus, Piscihepevirus en het (mogelijke) Hepelivirus (figuur 1). Met de ontdekking van zoönotische HEV begin jaren 90 van de vorige eeuw en de latere moleculaire fylogenie kon HEV worden onderverdeeld in genetische lijnen, waarbij de van oudsher bekende humane HEV wordt veroorzaakt door Orthohepevirus A genotype 1- en -2-virussen, terwijl daarnaast zoönotische infectie wordt veroorzaakt door Orthohepevirus A genotype 3- en -4-virussen.
Epidemiologie
Vooralsnog is het meeste onderzoek gedaan naar de humane genotypen 1-4. Genotype 1 en 2 komen vooral in ontwikkelingsgebieden voor in gebieden met minder hygiënische omstandigheden, waarbij vooral genotype 1 zich makkelijk via de feco-orale route en door mens-op-menscontact kan verspreiden. Genotype 1 is berucht als veroorzaker van grote uitbraken in situaties waarbij basishygiëne moeilijk kan worden nageleefd, zoals in vluchtelingenkampen, en door de hoge mortaliteit (15 tot 29 procent) onder zwangere vrouwen. Infecties met HEV-1 van niet-zwangeren zijn over het algemeen zelflimiterend, met een letaliteit van 0,2 tot 4 procent.
In geïndustrialiseerde landen werd HEV een decennium geleden vooral gezien als een importziekte, die reizigers in het buitenland opliepen. Onderzoek van de laatste jaren heeft echter duidelijk gemaakt dat ook deze Westerse landen (hyper)endemisch zijn voor HEV-genotype 3, van zoönotische herkomst. Genotype 3 is wereldwijd gevonden bij verschillende mogelijke reservoirdieren, zoals varkens, wilde zwijnen, herten, konijnen, geiten en mangoesten. Genotype 4 wordt vooral gevonden bij varkens in China en Japan, sporadisch ook in Europa (België); het is recent beschreven als oorzaak van een uitbraak via gecontamineerd kraanwater in China.2 Genotypen 5 en 6 zijn gevonden bij wilde zwijnen in Japan, maar tot zo ver bekend, niet bij de mens. Recent is ook HEV-genotype 7 (in eerste instantie uit dromedarissen geïsoleerd) gevonden bij een chronisch geïnfecteerde transplantatiepatient.3 De impact van zoönotische blootstelling aan genotype 7 moet nog verder worden onderzocht (figuur 2).
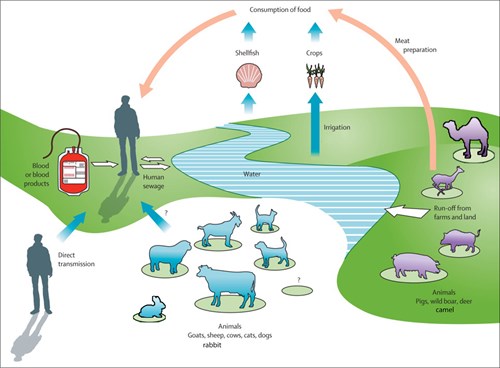
Ondanks dat HEV-3 bij veel verschillende diersoorten wordt gevonden, wordt het varken als primaire host beschouwd. HEV-3 wordt in grote hoeveelheden uitgescheiden in de feces van varkens (13 tot 59 dagen na infectie), waarbij vooral jonge biggen worden gezien als besmettingsbron met hoge transmissieratio’s (R0 = 8,8). Dat HEV-3 een globaal probleem is, is duidelijk. HEV-RNA wordt gevonden in oppervlakte en zeewater, irrigatiewater in Oost-Europa, op varkensboerderijen in Nederland (33 tot 55 procent), Italië (75 procent) en Canada.4-6 HEV-3-RNA is ook in de voedselketen aangetoond in varkenslevers en andere producten waarin (orgaan)vlees is verwerkt.7 In Engeland is in 10 procent van de worstjes HEV-RNA aangetoond, en in Frankrijk is transmissie aangetoond door het consumeren van een lokale lekkernij, de figatelliworst, waarin rauwe varkenslever verwerkt wordt.8 De consumptie van deze onvoldoende verhitte voedselwaren wordt gezien als verklaring voor de hoge seroprevalentie in Zuid-Frankrijk (52 procent).9 HEV wordt pas geïnactiveerd na een verhitting van 20 minuten bij 71°C.10
Ook transmissie via bloedtransfusie is beschreven. Een studie uit het Verenigd Koninkrijk (VK) laat echter zien dat het aantal besmettingen via bloedtransfusie relatief laag is, met 18 besmettingen op de 225.000 donaties.11 De kans op infectie in deze studie leek afhankelijk van virale lading en omgekeerd evenredig met antistoftiters van het donorbloed, en de ziektelast van HEV door bloeddonatie werd als laag beschouwd. Daarbij moet wel worden opgemerkt dat deze patiënten werden gevolgd en zo nodig werden behandeld, waardoor een grotere ziektelast is voorkomen. Daarnaast is de infectiedruk in Nederland (NL) hoger: er zijn circa 4,5 keer zoveel donoren HEV-viremisch als in het VK (1 op 762 in 2013-2014)12 en het aantal transfusiegerelateerde seroconversies is in Nederland circa 10 keer hoger dan in het VK (1,1 procent NL versus 0,1 tot 0,2 procent in het VK).
Deze infectiedruk lijkt in de afgelopen jaren zeker niet constant te zijn, zoals collega’s Hogema et al. laten zien in een seroprevalentiestudie in Nederland.13 Hierbij wordt in het totaal een seroprevalentie van 27 procent gevonden, die stijgt tot meer dan 40 procent bij mensen boven de 60 jaar. Daarnaast laat deze studie zien dat de seroprevalentie in de jongste donorengroep (18 tot 21 jaar) daalt vanaf 1988 tot 2000 (19,8 procent naar 4,3 procent) en daarna weer stijgt naar 12,7 procent in 2011, wat – in combinatie met het stijgende aantal HEV-viremische donoren – zou kunnen worden geïnterpreteerd als een stijgende infectiedruk. De oorzaak van die dynamiek in HEV-infecties is onduidelijk. Een mogelijke verklaring is dat de epidemiologie van HEV-3 bij varkens is veranderd. Een recent gepubliceerde experimentele studie toonde aan dat HEV bij varkens na infectie met het veelvoorkomend Porcine Reproductive and Respiratory Syndrome-virus aanzienlijk langer wordt uitgescheiden.14 Dat betekent dat co-circulatie van andere pathogenen de kans op aanwezigheid van HEV bij varkens op de slachtleeftijd (zes maanden) kan vergroten. Of dit inderdaad een rol speelt in de veranderde incidentie van humane HEV-infecties is niet duidelijk.
Kliniek, diagnostiek en behandeling
Bij immuuncompetente individuen is HEV voornamelijk een zelflimiterende asymptomatische virusinfectie, met een incubatieperiode van vier tot zes weken, die veelal niet hoeft te worden behandeld. In sommige gevallen verloopt de infectie fulminant met acuut leverfalen als gevolg. Daarnaast zijn er extrahepatische symptomen gerapporteerd.15 Vooral (zeldzame) neurologische symptomen zoals het guillain-barrésyndroom en brachiale neuritis zijn in verband gebracht met een acute HEV-infectie en worden mogelijk veroorzaakt door moleculaire mimicry, waardoor een immuunrespons tegen lichaamseigen moleculen wordt geactiveerd.16,17 Dit vraagt echter nog meer mechanistisch onderzoek, want virale replicatie bij bijvoorbeeld brachiale neuritis is niet uitgesloten, aangezien HEV wel in vitro lijkt te repliceren in neurale cellijnen.18
Het beloop van virale hepatitis door HEV is een belangrijk samenspel tussen het immuunsysteem van de gastheer, immuunpathologie en de hepatische reserve.19 HEV-infectie veroorzaakt zowel een humorale als een cellulaire respons. Na infectie zijn IgM- en IgG-antistoffen aantoonbaar in bloed, waarbij IgG tot 23 jaar kan persisteren.13 De CD4+/CD8+-T-cellen worden geactiveerd, wat leidt tot productie van interferon-γ, TNF-α en IL-2 cytokines. Een jaar na infectie neemt het aantal CD4+-cellen en de polyfunctionaliteit van de CD8+-cellen echter sterk af. De afnemende immuunrespons zou een verklaring kunnen zijn voor de secundaire infecties bij HEV-IgG+-patiënten.20 Ook deze secundaire infecties kunnen bij immuungecompromitteerde patiënten leiden tot een chronische infectie.21 Verder zien we vooral dat patiënten met een verminderde leverfunctie een risico lopen op een ernstiger beloop van de infectie, een zogeheten 'acute-on-chronic' HEV-infectie.
Wanneer immuungecompromitteerde patiënten, zoals transplantatiepatiënten, worden geïnfecteerd, wordt de HEV-3-infectie − zonder behandeling − bij 60 tot 80 procent van deze patiënten chronisch. Vooral immuunsuppressieve middelen die T-celsignaleringen en daarmee IL-2-productie onderdrukken, zijn een risicofactor voor een chronisch beloop van de infectie.22,23 De humorale respons van immuun-gecompromitteerden komt niet of later op gang, waardoor serologie bij deze patiëntengroep minder betrouwbaar is en een (kwantitatieve) HEV-PCR de diagnostiek van keuze is om infectie vast te stellen en te monitoren. HEV kan bij deze patiëntengroep snel een agressief beloop hebben; bij vier van de zes harttransplantatiepatiënten werd binnen een jaar gevorderde fibrose gediagnosticeerd.24 Om deze reden is snelle interventie nodig. In eerste instantie kan worden gepoogd om de immuunsuppressie te verlagen, wat bij 30 procent van de patiënten voldoende is om de infectie te klaren. Er kan echter een dilemma ontstaan, aangezien dit bij solide orgaantransplantatiepatiënten de kans op afstoting van het transplantaat vergroot en bij de stamceltransplantatiepatiënten de kans op graft-versus-hostziekte (GVHD) verhoogt. Daarnaast is GVHD van de lever bij deze laatste patiëntengroep niet te onderscheiden van een adequate immuunrespons tegen HEV in de lever na (gedeeltelijke) immuunreconstitutie; beide geven leverenzymstijgingen. Wanneer na drie maanden de immuunsuppressie niet verder kan worden verlaagd en de infectie nog niet is geklaard, kan worden overwogen om ribavirine te starten, wat in 75 tot 85 procent van de gevallen succesvol is. Belangrijk is om de virale lading van HEV tijdens het afbouwen van de immuunsuppressie of therapie nauw te volgen. Behandeling met ribavirine duurt gemiddeld drie maanden. Het advies is om pas te stoppen met behandeling indien het HEV-RNA niet meer detecteerbaar is in plasma en feces. Voor de overige 15 tot 25 procent van de gevallen is er op dit moment geen beter alternatief dan (langere) herbehandeling met ribavirine.19
One health voor betere voedselveiligheid
Zowel de aanwezigheid van HEV-3 in de omgeving en de voedselketen als de onduidelijkheid wat het meest bijdraagt aan infecties en ziekte bij de mens, vragen om onderzoek en bestrijding en daarmee om samenwerking tussen organisaties die verantwoordelijk zijn voor medische, veterinaire, en publieke gezondheidszorg, voor milieubeheer en voedselveiligheid. Er is onderzoek nodig naar de bijdrage van de verschillende mogelijke transmissieroutes aan de incidentie van HEV bij de mens. Dat onderzoek kan gerichte preventie- en interventiemaatregelen onderbouwen. De transmissie beperken zou mogelijk moeten zijn door vaccinatie. Afhankelijk van het genotype zou overwogen kunnen worden om varkens (genotype 3, weinig mens-op-menstransmissie, maar wel in de voedselketen) en mensen (genotype 1, transmissie-events die zijn gerelateerd aan humane feco-orale uitbraken, transplantatiepatiënten voor genotype 3) te vaccineren. Er is op dit moment echter maar één (recombinant) HEV-vaccin op de markt (in China, sinds 2012). Dit vaccin is gericht tegen genotype 1 en is vooralsnog niet in de rest van de wereld verkrijgbaar. Ondanks dat het vaccin voor genotype 1 is ontwikkeld, lijkt het ook voor genotype 3 te werken. Voor zover bekend hebben alle genotypen die tot de species Orthohepevirus A horen één serotype.
Interventie door de kans op HEV-transmissie te verkleinen kan op verschillende niveaus: transmissie vanuit het reservoir (in dit geval in eerste instantie varkens) kan worden beperkt door te adviseren om geen rauwe vleeswaren te consumeren en geen producten te eten die niet zodanig zijn bewerkt dat eventueel aanwezige virussen geïnactiveerd worden (bijvoorbeeld door middel van inzouten). Transmissie via bloedproducten kan worden voorkomen door bloeddonoren te screenen (Japan, Ierland, Verenigd Koninkrijk, Nederland vanaf juli 2017) of op specifieke bloedproducten met (mogelijk) hoger transmissierisico, zoals plasmapools (Frankrijk, Duitsland) of met detergentia behandeld plasma.25,26 De bewerking van plasma met detergentia kan juist de infectiviteit verhogen, aangezien de vorm van HEV (namelijk mét envelop) die voorkomt in perifeer bloed, minder infectieus is dan het HEV-virion zonder envelop, dat in feces wordt uitgescheiden.27 Wanneer HEV-besmet plasma echter wordt behandeld met detergentia, wordt deze envelop chemisch verwijderd, wat deze plasmaproducten mogelijk meer infectieus maakt. Voor risicogroepen is het ook belangrijk om surveillance te verhogen en een ‘search and destroy’-strategie toe te passen. Dit kan in het kader van patiëntenzorg, zoals (jaarlijkse) screening van transplantatiepatiënten op aanwezigheid van HEV-RNA. Door deze screening zijn in enkele jaren meer dan 32 nieuwe HEV-geïnfecteerde patiënten geïdentificeerd in het Erasmus MC (40,5 procent (n = 32) van het totaal aantal HEV-cases (n = 79)),28 die allen succesvol zijn behandeld.
De onderliggende vraag is of het nodig is om HEV-3 bij varkens te bestrijden. Aangezien de infectie bij deze dieren asymptomatisch verloopt en zeer wijdverbreid is, is de bereidwilligheid vanuit de varkenshouderij nihil. Vanwege de mogelijke rol van co-infecties op de epidemiologie van HEV bij varkens en het indirecte effect op risico voor de mens, is het zinvol om deze hypothese te onderzoeken. Aangezien er aanwijzingen zijn voor verschillen in virulentie tussen HEV-genotypen, is het belangrijk om de genetische diversiteit van HEV bij dieren en mensen goed te monitoren. Daarbij is het raadzaam om mogelijkheden te verkennen voor gebruik van ‘catch-all’-methoden zoals 'high-throughput next generation sequencing' met 'random amplification' of 'random viral capture'. Het grote voordeel is dat er meer pathogenen kunnen worden gedetecteerd, wat kosteneffectiever is. Het belangrijkste voor de bestrijding van deze en andere zoönosen is echter de steun vanuit hogere bestuurlijke kringen, waaronder de politiek, die middelen ter beschikking kan stellen om de eerdergenoemde interventieacties te bewerkstelligen en die gezondheidszorgers kan bewegen tot samenwerking.
Dankbetuiging
Dit manuscript is ondersteund door het Netherlands Centre for One Health (NCOH).